Creen una nova estratègia d'alliberament de fàrmacs antitumorals contra el càncer de mama
20/11/2019
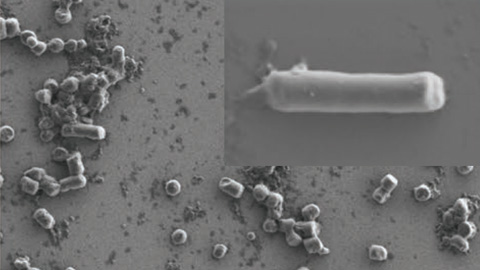
L'alliberament local de fàrmacs antitumorals a través de proteïnes bacterianes per al tractament de càncer de mama pot marcar un abans i un després en la medicina de precisió. En aquesta línia, investigadors del CIBER de Bioenginyeria, Biomaterials i Nanomedicina (CIBER-BBN), de la Universitat Autònoma de Barcelona, del Vall d’Hebron Institut de Recerca i del CSIC han creat estructures de cèl·lules d'Escherichia coli per produir amiloides bacterians no tòxics. Els cossos d'inclusió o amiloides són agregats de proteïnes nanoestructurades produïdes a l'interior d'una cèl·lula, freqüents en determinat bacteris, i amb interessants aplicacions biomèdiques, com ara l'alliberament de fàrmacs proteics, com és el cas.
Aquestes estructures proteiques actuen com a grànuls de secreció dels fàrmacs antitumorals, i en ser administrats localment mostren un efecte terapèutic sostingut en el temps. Si bé aquesta investigació, publicada a Advanced Science està en les primeres fases de desenvolupament, el principi transversal descrit en l'estudi obre un ampli camp d'experimentació per a la generació de nous biomaterials terapèutics produïts en bacteris, per a la medicina de precisió de càncer de mama i en altres neoplàsies d'elevada incidència.
Aquest projecte d'investigació, finançat per la fundació La Marató de TV3, ha estat coordinat per la investigadora de l'CIBER-BBN de la UAB Esther Vázquez, i ha comptat a més amb la participació d'Ibane Abasolo (Hospital Vall d'Hebron) i de Miriam Royo (CSIC). Així mateix, el consorci ha comptat amb la col·laboració de Laura Soucek, experta en models animals per a l'estudi del càncer i pertanyent a la Vall d'Hebron Institut d'Oncologia (VHIO) i ICREA.
Segons explica Esther Vázquez, "tot i que aquesta tecnologia encara té un llarg recorregut fins a la seva aplicació clínica, els resultats obtinguts en aquest estudi, que ha durat més de tres anys, obren les portes a una nova tecnologia terapèutica basada en productes bacterians fins ara no explorats en clínica".
L'estudi es basa en el lliurament dirigit a cèl·lules tumorals CD44 +, en models animals de càncer de mama, de dues proteïnes antitumorals, Omomyc i p31, en forma de materials nanoestructurats. La principal novetat de l'estudi resideix en l'ús d’amiloides bacterians no tòxics com a reservori d'aquestes proteïnes terapèutiques. L'administració local del material promou l'alliberament sostingut dels fàrmacs i la necrosi del teixit tumoral en un marge de temps relativament curt. Un dels principals avantatges en l'ús d'aquests tipus de materials és l’alliberament sostingut del fàrmac proteic, el que disminuiria la freqüència d'administració en relació a les pautes actuals dels fàrmacs convencionals.
El projecte ha comptat a més amb la col·laboració dels caps de grup del CIBER-BBN Antonio Villaverde, de la UAB, expert en el desenvolupament de materials bacterians d'interès biotecnològic basats en estructures amiloides, conegudes també com a cossos d'inclusió, i de Simó Schwartz, director del CIBBIM-Nanomedicine (VHIR), expert en nanomedicina i biologia molecular del càncer.
Article de referència:
Mireia Pesarrodona, Toni Jauset, Zamira V. Díaz‐Riascos, Alejandro Sánchez‐Chardi, Marie‐Eve Beaulieu, Joaquín Seras‐Franzoso, Laura Sánchez‐García, Ricardo Baltà‐Foix, Sandra Mancilla, Yolanda Fernández, Úrsula Rinas, Simó Schwartz Jr, Laura Soucek , Antonio Villaverde, Ibane Abasolo, Esther Vázquez. Targeting Antitumoral Proteins to Breast Cancer by Local Administration of Functional Inclusion Bodies, Advanced Science. https://doi.org/10.1002/advs.201900849