Dissenyen nanoenzims amb una combinació única d'estructura i funcions
Un equip de recerca de la UAB ha dissenyat unes bioestructures mínimes capaces de realitzar dues activitats enzimàtiques diferenciades i regulables de manera reversible gràcies a una combinació única de propietats estructurals i funcionals. L'estratègia utilitzada obre la porta a la creació de nanomaterials “intel·ligents” amb combinacions a la carta de funcions catalítiques.
04/03/2021
Hi ha un interès creixent per dissenyar sistemes biològics sintètics que puguin executar reaccions químiques inspirades en els enzims, sense requerir les complexes estructures que els caracteritzen. Una de les aproximacions que més s'està explorant és l'autoassemblatge de pèptids -molècules més petites que les proteïnes-, per la seva biocompatibilitat i pel control que permeten sobre les seves propietats estructurals i funcionals.
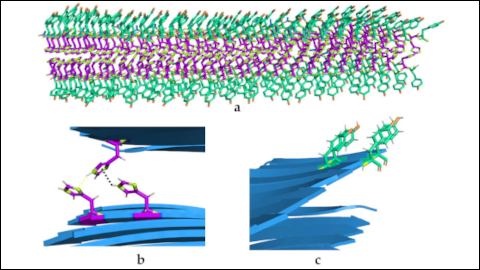
Un equip de recerca de la UAB, liderat per l'Institut de Biotecnologia i Biomedicina de la (IBB), ha dissenyat recentment una de les estructures mimètiques d'enzims més petites descrites fins ara. Es tracta de pèptids d'entre 7 i 9 aminoàcids que s'autoassemblen espontàniament per formar fibres de tipus amiloide estables i hidrogels sòlids, innocus per a les cèl·lules.
Els pèptids estan formats únicament per 2 tipus d'aminoàcids hidrosolubles (tirosina i histidina), un codi binari que conté tota la informació per formar les nanoestructures. A més, són reversibles i poden realitzar dues activitats catalítiques diferenciades i no relacionades entre si.
Els investigadors han aconseguit un sistema més simple i controlable de l'activitat enzimàtica i, per primera vegada, una estructura en què els mateixos aminoàcids que proporcionen l'activitat catalítica contribueixen també a formar el bastiment macromolecular. En treballs anteriors aquestes capacitats estaven segregades en diferents regions de la molècula, la qual cosa resultava en pèptids més llargs i, o, amb una única activitat.
“El quid de la qüestió és que l'activitat catalítica de fibres i hidrogels només s'aconsegueix quan els pèptids s'autoassemblen”, explica Salvador Ventura, que ha coordinat l'estudi. “L'estratègia que hem utilitzat estableix les bases per generar materials nanoestructurats intel·ligents, amb combinacions a la carta de funcions catalítiques per a nombroses aplicacions pràctiques”.
Propietats úniques
Fins ara, a la majoria de pèptids mínims dissenyats els faltava una de les capacitats més importants dels enzims naturals: la de regular la seva activitat de manera reversible. En aquest estudi els investigadors ho han aconseguit controlant la capacitat d'assemblatge, fet que permet alternar formes actives i inactives amb simples canvis de pH.
Els nous pèptids tenen, a més, propietats que no tenen els enzims naturals. Aquests realitzen només una activitat catalítica. Ara han aconseguit que incorporin dues activitats diferents (hidrolítiques i electrocatalítiques) que poden realitzar-se simultània o alternativament. En un altre cas això requeriria dos enzims artificials estructuralment diferents i centenars de vegades més grans i cars.
Una altra característica dels nous enzims artificials que destaquen els investigadors és que l'autoassemblatge és espontani, fet pel qual no requereix reactius químics addicionals o l'aplicació de calor, que podrien resultar tòxics o tenir conseqüències dràstiques en l'estructura.
Major eficiència i economia
Els hidrogels i fibres tipus amiloide resultants permeten generar microreactors sòlids de gran eficiència i economia, en què el producte final de la reacció es pot separar fàcilment de l'enzim artificial.
“Les estructures macromoleculars que hem aconseguit poden tenir aplicacions importants en microfluídica i també en drug-delivery, ja que poden encapsular el fàrmac en estat assemblat i alliberar-lo de manera específica, una vegada aconseguit el context cel·lular adequat, simplement desmuntant l’assemblatge”, destaca Salvador Ventura.
L'investigador lidera el grup de Malalties del plegament de proteïnes i de la conformació a l’IBB. “Les línies de recerca nanotecnològiques les hem iniciat fa només tres anys, però el coneixement del mecanisme molecular de l'assemblatge de proteïnes en estructures amiloides ens està facilitant desenvolupar nous nanomaterials sintètics funcionals amb propietats que no es poden aconseguir amb proteïnes o pèptids naturals”, assenyala.
En l‘estudi, publicat a la revista ACS Catalysis, han participat investigadors de l’IBB i dels Departaments de Química i de Bioquímica i Biologia Molecular de la UAB (Salvador Ventura, Marta Díaz-Caballero, Susanna Navarro, Mariona Sodupe i Luis Rodríguez-Santiago); de l'Institut de Ciència de Materials de Barcelona (ICMAB-CSIC) (Francesc Teixidor i Miquel Nuez-Martínez) i del CIC bioGUNE (Francesca Peccati).
Referència: Marta Díaz-Caballero, Susanna Navarro, Miquel Nuez-Martínez, Francesca Peccati, Luis Rodríguez-Santiago, Mariona Sodupe, Francesc Teixidor, and Salvador Ventura. pH-Responsive Self-Assembly of Amyloid Fibrils for Dual Hydrolase-Oxidase Reactions. ACS Catalysis 2021 11 (2), 595-607. DOI: 10.1021/acscatal.0c03093