Avance en la lucha contra un patógeno hospitalario muy resistente a los antibióticos
Una investigación con participación de la UAB halla un nuevo mecanismo por el cual Acinetobacter baumannii es capaz de adquirir resistencias a los antibióticos.
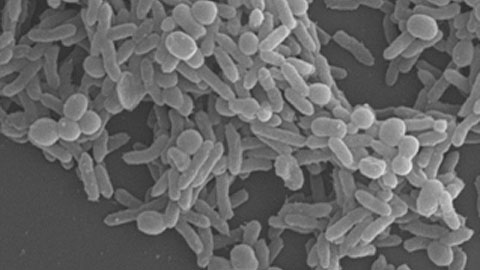
Acinetobacter baumanniies una bacteria que puede formar parte de la microbiota normal de la piel de las personas sanas. Sin embargo, los pacientes hospitalizados, especialmente los enfermos críticos que se encuentran en las unidades de cuidados intensivos, son susceptibles de ser infectados por este microorganismo, que puede provocar infecciones graves como septicemia, neumonía o meningitis.
Una de las principales problemáticas que presenta A. baumannii es su gran capacidad de desarrollar resistencias a prácticamente todos los antibióticos en uso clínico. En este estudio, los investigadores han identificado los genes del sistema SOS responsables del incremento de la mutagénesis de la bacteria y el mecanismo por el cual este incremento tiene lugar.
El sistema SOS es una respuesta global de reparación del DNA que tienen las bacterias y que se dispara cuando se lesiona su material genético. Una de las consecuencias de la inducción del sistema SOS es el aumento de la frecuencia de mutagénesis en las células bacterianas. Esto es debido a que ante la situación de estrés les produce el daño masivo en el DNA, las bacterias prefieren cometer errores en la copia de su material genético antes de que dejar éste sin reparar y afrontar su muerte. En la mayoría de bacterias estudiadas, la proteína RecA juega un papel central en la reparación del DNA, tanto directamente, mediante procesos de recombinación, como indirectamente, a través de la regulación de esta respuesta.
Los científicos han evidenciado que A. baumannii posee tres DNA polimerasas con una elevada tendencia al error en la copia de su DNA cuando se induce el sistema SOS y que incrementan su tasa de mutagénesis en presencia de varios antibióticos de uso clínico, como por ejemplo quinolonas y aminoglucósidos. Este aumento de la frecuencia de mutagénesis, que se ha demostrado que depende de la actividad de la propia proteína RecA de A. baumannii, es uno de los responsables del alto nivel de la aparición de mutantes resistentes a varios antibióticos que presenta la bacteria a nivel hospitalario.
Durante la investigación también han podido demostrar que los antibióticos que pertenecen a los grupos de los carbapenemes y la colistina no inducen el aumento de la tasa de mutagénesis y que, por tanto, es recomendable su utilización conjunta para aminorar el efecto estimulador de muchos antibióticos sobre la generación de cepas resistentes a ellas mismas.
Los datos obtenidos abren las puertas al diseño tanto de inhibidores de la proteína RecA de A. baumannii como de sus DNA polimerasas tendentes al error que, utilizados como coadyuvantes terapéuticos, podrían reducir la aparición de resistencias a los antibióticos, facilitando así el tratamiento de las infecciones causadas por la bacteria.
La investigación ha sido realizada por los doctores Jordi Barbé, Jesús Aranda y Pilar Cortés, del Grupo de Microbiología Molecular del Departamento de Genética y Microbiología de la UAB, en el marco de un proyecto conjunto con el Servizo de Microbioloxia-INIBIC del Hospital de A Coruña dirigido por el Dr. Germán Bou y con la colaboración del grupo australiano de la Monash University, dirigido por los doctores Ben Adler y John D. Boyce.
Los trabajos de investigación han generado dos publicaciones en la revista Journal of Bacteriology y dos más en la revista Antimicrobial Agentes and Chemotherapy de la American Society for Microbiology.
Artículos de referencia:
Jesús Aranda; Carlota Bardina; Alejandro Beceiro; Soraya Rumbo; Maria P Cabral; Jordi Barbé; Germán Bou. Acinetobacter baumanniiRecA protein in repair of DNA damage, antimicrobial resistance, general stress response, and virulence. Journal of bacteriology. 2011.
Jesús Aranda; Margarita Poza; Miguel Shingu Vázquez; Pilar Cortés; John D Boyce; Ben Adler; Jordi Barbé; Germán Bou. Identification of a DNA-damage-inducible regulon in Acinetobacter baumannii. Journal of bacteriology. 2013.
Alejandro Beceiro; Antonio Moreno; Nathalie Fernández; Juán A Vallejo; Jesús Aranda; Ben Adler; Marina Harper; John D Boyce; Germán Bou. Biological Cost of Different Mechanisms of Colistin Resistance and Their Impact on Virulence in Acinetobacter baumannii. Antimicrobial agents and chemotherapy. 2014.
Jesús Aranda; Mario López; Enoy Leiva; Andrés Magán; Ben Adler; Germán Bou; Jordi Barbé. Role of Acinetobacter baumannii UmuD homologs in antibiotic resistance acquired through DNA-damage-induced mutagenesis. Antimicrobial agents and chemotherapy. 2014.