Una recerca en col·laboració amb el Sincrotró ALBA prova la ineficàcia d'alguns fàrmacs contra la diabetis
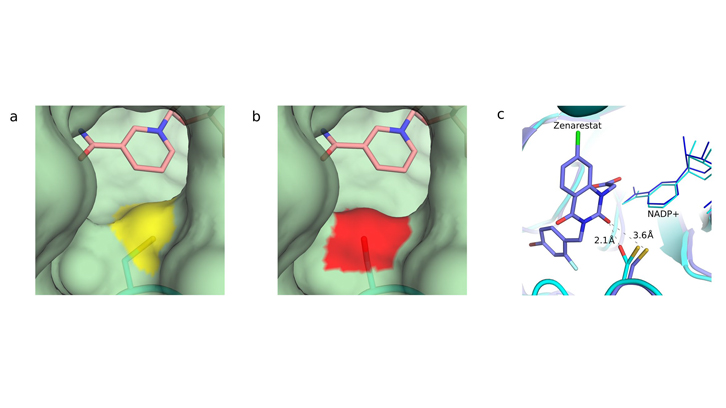
Figura 1. Canvis en el canal d'entrada al centre d’unió de l’aldosa reductasa. La conversió de la cisteïna en serina modifica l'entrada del substrat (glucosa). a) Entrada del centre d'unió de la forma nativa de l'aldosa reductasa. L'àtom de sofre de la cisteïna està marcat en groc. b) Entrada del centre d'unió de la proteïna irradiada, que mostra la serina en vermell. En tots dos casos, l’anell de nicotinamida del cofactor involucrat s’indica en color rosa. c) Col·lisions estèriques de l’aldosa reductasa activada amb un dels fàrmacs provats: el Zenarestat. L’inhibidor, dissenyat contra la forma nativa, mostra col·lisions severes amb la serina però no amb la cisteïna.
L’aldosa reductasa és una proteïna que s’estudia des dels anys 80 i ja fa temps que es coneix la seva relació amb la diabetis. Ara, els investigadors Xavier Parés i Jaume Farrés, en col·laboració amb l’equip del Sincrotró ALBA, han demostrat per què alguns dels fàrmacs que s’estan desenvolupant per tractar els efectes de la diabetis no funcionen en l’intent de bloquejar l’aldosa reductasa. Els resultats d’aquesta recerca s’han publicat a la revista Scientific Reports.
Per evitar aquesta situació, cal obtenir un fàrmac que inhibeixi l’activitat de l’aldosa reductasa per reduir la presència de sorbitol. L’objectiu és que el fàrmac s’uneixi a la proteïna i ocupi el lloc d’enllaç que correspondria a la glucosa. Així, s’aturaria d’arrel la reacció química que porta a l’estrès oxidatiu.
Tanmateix, encara no s’han creat fàrmacs efectius per combatre la proteïna i en els assajos clínics no funcionen com seria desitjable. “La qüestió és que l’aldosa reductasa pot presentar dues formes diferents, la nativa original i l’activada. Degut a l’estrès oxidatiu que hi ha en condicions de diabetis, canvia de forma i apareix la variant activada” explica Isidro Crespo, estudiant de doctorat del Sincrotró. Malgrat saber-se aquest canvi en l’estructura de la proteïna, se segueixen dissenyant fàrmacs tenint en compte la forma original, enlloc de l’activada. Els resultats obtinguts per l’equip mostren en detall com canvia la proteïna sota els efectes de l’estrès oxidatiu i, el més important, com aquests canvis afecten l’eficàcia dels fàrmacs.
Nou mètode amb llum de sincrotró
La línia de llum XALOC del Sincrotró ALBA permet determinar quina estructura tridimensional tenen les proteïnes. En aquest estudi, a més, també s’ha aprofitat la llum de sincrotró, principalment formada per raigs X d’alta energia, per produir danys a la proteïna. “Hem vist que, irradiant l’aldosa reductasa amb la llum del Sincrotró, podem provocar els mateixos efectes que els que pateix la proteïna sota l’estrès oxidatiu de les cèl·lules de persones amb diabetis” comenta Albert Castellví, investigador de l’equip. “Aconseguim convertir la forma nativa de la proteïna en una altra que es comporta igual que la forma activada real que tenen els diabètics” afegeix.
Un cop obtinguda aquesta forma activada, han provat fàrmacs que ja havien estat descartats en els assajos clínics i han corroborat que no són efectius. Conclouen que es deu al canvi d’estructura que ha patit la proteïna a causa de la irradiació amb els raigs X del Sincrotró. Sota condicions d’estrès oxidatiu, la conversió de tan sols un aminoàcid de la proteïna original (una cisteïna) en d’altres aminoàcids, majoritàriament serina o alanina, afecta la unió del fàrmac inhibidor a la proteïna i explica el canvi de comportament dels fàrmacs. Perquè el fàrmac sigui efectiu, cal que encaixi en l’aldosa reductasa com si es tractés d’una peça d’un trencaclosques. Si la proteïna canvia de forma, el fàrmac no hi encaixarà bé. Per als investigadors, aquest fet causa la ineficàcia dels fàrmacs de la diabetis i proposen obrir una nova via en el desenvolupament de fàrmacs: dissenyar-los perquè encaixin en la forma canviada, l’activada, per bloquejar-la totalment.
L’alta complexitat de l’estrès oxidatiu i la diversitat de factors que el provoquen fan que no es pugui reproduir in vitro. “Per això el mètode amb llum de sincrotró és de gran utilitat per induir i estudiar els canvis que pateix l’aldosa reductasa en les condicions d’estrès oxidatiu derivades de la diabetis”, ressalta Judith Juanhuix, investigadora i responsable d’aquest estudi. Aquest mètode, de fet, és generalitzable i es podria estendre a l’estudi d’altres proteïnes que veuen modificada la seva estructura en estrès oxidatiu i que són rellevants en malalties com el Parkinson, el càncer o l’Alzheimer.
Universitat Autònoma de Barcelona
Referències
Castellví A, Crespo I, Crosas E, Cámara-Artigas A, Gavira JA, Aranda MAG, Parés X, Farrés J, Juanhuix J. (2019). Efficacy of aldose reductase inhibitors is affected by oxidative stress induced under X-ray irradiation. Sci Rep, 9(1):3177. DOI: 10.1038/s41598-019-39722-0.


