El descobriment d'un mecanisme de defensa contra fags a Salmonella obre nous reptes per a l'aplicació de la teràpia fàgica
La teràpia fàgica, l’ús de virus que infecten bacteris, es considera una estratègia prometedora per al tractament de les infeccions bacterianes. Malgrat això, s’enfronta al repte que els bacteris poden desenvolupar mecanismes sofisticats per defensar-se'n. Personal investigador de la UAB ha identificat un nou mecanisme de defensa a Salmonella adquirit per transferència lateral a l’intestí de pollastres d’engreix tractats amb teràpia fàgica oral.
Investigadors del Grup de Microbiologia Molecular del Departament de Genètica i de Microbiologia de la UAB, liderats per la Dra. Montserrat Llagostera, han publicat un estudi pioner que descriu un nou mecanisme de defensa adquirit per transferència lateral a Salmonella, que condueix a una disminució en l'expressió de proteïnes estructurals i de la lisi cel·lular del bacteriòfag UAB_Phi20 i culmina en una infecció abortiva.
En els darrers anys, la teràpia fàgica s’ha consolidat com una estratègia fonamental per al tractament d’infeccions bacterianes causades per patògens que han desenvolupat resistència múltiple als antimicrobians convencionals. No obstant això, la coevolució entre bacteriòfags i bacteris ha donat lloc a una gran varietat d’estratègies bacterianes per contrarestar la infecció fàgica, fet que representa un repte important per a l’aplicació extensiva d’aquesta teràpia en l’àmbit de la salut humana i animal. L’estudi d’aquests mecanismes de defensa és clau per comprendre la relació entre fags i bacteris, així com per garantir un ús segur de la teràpia fàgica.
En aquest context, el treball recentment publicat representa un estudi innovador en identificar el gen ibfA com un nou factor de defensa en Salmonella enterica serotip Typhimurium davant el fag virulent UAB_Phi20. Aquest descobriment és especialment rellevant, ja que el gen no està codificat en el genoma bacterià, sinó que ha estat identificat en un plasmidi conjugatiu del grup IncI1α, adquirit per Salmonella mitjançant transferència lateral a l’intestí de pollastres d’engreix durant un tractament amb teràpia fàgica oral.
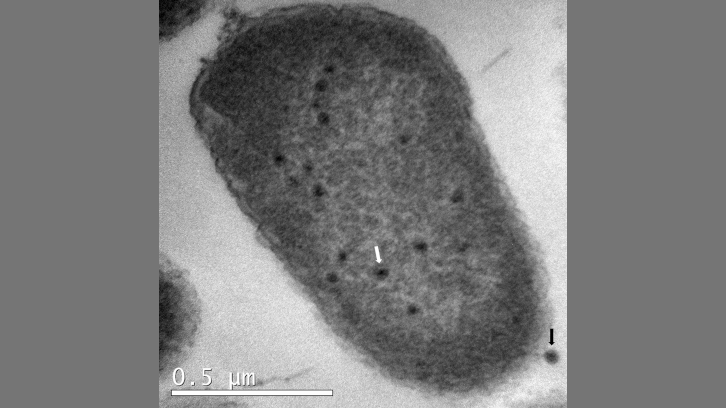
Mitjançant un enfocament metodològic basat en microbiologia molecular, tècniques microbiològiques convencionals, microscòpia electrònica de transmissió (TEM) i bioinformàtica, s’ha caracteritzat la funció del gen ibfA, que codifica una proteïna amb dos dominis de tipus ATPasa i TO-PRIM. L’expressió d’IbfA redueix significativament la infectivitat i la productivitat del fag UAB_Phi20. Aquest efecte s’evidencia per la disminució de l’eficiència de plaqueig (EOP), l’eficiència de formació de centres infectius (ECOI) i la mida de l’explosió fàgica, sense observar-se una lisi cel·lular evident, tot i que sí una menor viabilitat cel·lular.
En l'àmbit molecular, s’ha observat que ibfA altera el procés de transcripció del genoma del fag i afavoreix l’expressió dels gens primerencs del fag, com l’antirepressor ant, cosa que provoca un desequilibri entre les proteïnes reguladores Cro i C2. Aquest desequilibri condueix a una reducció en l’expressió de proteïnes estructurals del fag i de la lisi cel·lular i acaba provocant una infecció de tipus abortiu, un efecte que podria estendre’s a altres fags del tipus P22.
A més, malgrat l’origen evolutiu incert d’ibfA, aquest gen es troba àmpliament distribuït tant en cromosomes com en plasmidis de procariotes. Això suggereix que podria exercir funcions addicionals beneficioses per a les cèl·lules bacterianes, més enllà de la defensa contra fags.
Departament de Genètica i Microbiologia
Universitat Autònoma de Barcelona
Referències
López-Pérez, J.; Cortés, P.; Campoy, S.; Erill, I.; Llagostera, M. (2025). Deciphering the causes of ibfA-mediated abortive infection in the P22-like phage UAB_Phi20. International Journal of Molecular Sciences 26(10): 4918. https://doi.org/10.3390/ijms26104918


