El medio de cultivo de las micobacterias terapéuticas afecta su eficacia en el tratamiento contra el cáncer de vejiga
El actual tratamiento para el cáncer de vejiga no invasivo consiste en provocar una respuesta antitumoral en el organismo instilando la micobacteria Mycobacterium bovis Calmette-Guérin (BCG) en la vejiga. Investigadoras del Departamento de Genética y Microbiología de la UAB han estudiado qué medios de cultivo para crecer BCG mejoran la respuesta antitumoral del organismo, así como la respuesta si se instila Mycobacterium brumae.
El tratamiento de elección para el cáncer de vejiga (CV) no invasivo consiste en la resección del tumor seguida de instilaciones dentro de la vejiga de una bacteria, Mycobacterium bovis Calmette-Guérin (BCG), que también se usa como vacuna para prevenir la tuberculosis. Aun siendo el tratamiento más eficaz para evitar la recurrencia y progresión del tumor, el 30% de los pacientes no responden a esta terapia, y alrededor del 70% de los enfermos sufren efectos adversos. De hecho, el 8% de ellos tiene que interrumpir el tratamiento quedándose con escasas alternativas terapéuticas.
El mecanismo de acción del BCG así como los antígenos implicados en la respuesta antitumoral no se conocen, lo que implica que se desconozcan qué pacientes responderán favorablemente o no al tratamiento com BCG. De hecho, el perfil antigénico del BCG podría ser modificado en función del medio de cultivo utilizado para su crecimiento y, en consecuencia, podría alterar su efecto antitumoral. En este sentido, se ha observado que el medio de cultivo puede afectar en la respuesta producida de la BCG como vacuna para la tuberculosis. Las condiciones de cultivo del BCG son de relevante importancia ya que la producción de BCG a escala industrial alrededor del mundo se lleva a cabo usando distintas formulaciones del medio de cultivo, pudiendo afectar al efecto antitumoral, y siendo un parámetro clave para entender el éxito del tratamiento. Por otro lado, y en busca de una alternativa más segura y/o eficaz al tratamiento con la BCG, se ha descrito el efecto antitumoral de otra micobacteria, Mycobacterium brumae. M. brumae es una micobacteria ambiental, no patógena y de crecimiento rápido que ha demostrado capacidad inmunoterapéutica en estudios preclínicos.
El objetivo principal de nuestros estudios fue determinar si la actividad antitumoral de BCG y de M. brumae se veía modificada en función del medio de cultivo usado para el crecimiento de las micobacterias. Las micobacterias se hicieron crecer en el medio Middlebrook, y tres composiciones diferentes del medio Sauton usadas por fabricantes de BCG: Sauton-A60, Sauton-G15 i Sauton-G60. Posteriormente, las micobacterias crecidas en las diferentes condiciones de cultivo se utilizaron como terapia antitumoral en el modelo ortotópico de ratón de CV.
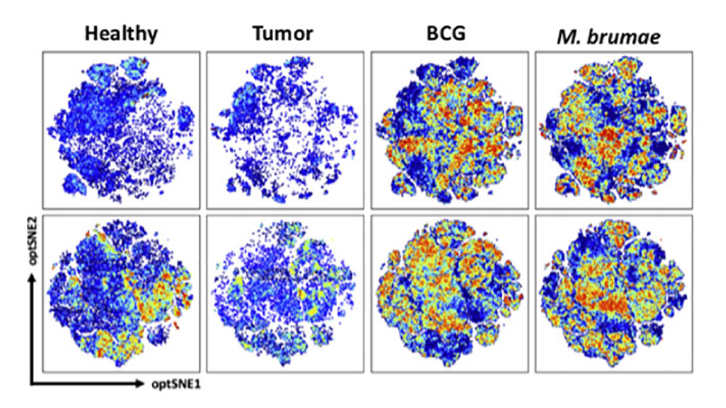
Los resultados mostraron que cada micobacteria necesita un medio de cultivo específico para maximizar su actividad. Específicamente, M. brumae crecido en Sauton-A60 y BCG crecido en Sauton-G15 consiguieron mejores resultados en cuanto a la eliminación del tumor que el resto de formulaciones. Cabe destacar que M. brumae-A60 fue el más eficaz entre todos los tratamientos probados, incluyendo todas las condiciones del BCG. Mostró una mayor actividad citotóxica de las células del sistema inmune en frente de células tumorales y la mayor producción de interleucina IL-17 e interferón gamma IFN-ɣ a nivel sistémico. Con M. brumae-A60 se observó una infiltración específica y moderada de células inmunitarias importantes para eliminar el tumor de la vejiga: infiltración de celulas linfoides innatas y linfocitos T CD4. BCG-G15 desencadenó una infiltración masiva de células inmunitarias, principalmente linfocitos T CD3 (CD4 y CD8) y células T Natural Killer (NKT), entre otras; además de una elevada producción de IFN-ɣ a nivel sistémico (Guallar-Garrido et al., 2022; Senserrich et al., 2022).
El análisis de la pared celular de BCG y de M. brumae crecidas en los distintos medios de cultivo demostró que las fórmulas más eficaces, M. brumae-A60 y BCG-G15, presentaban una menor variedad de lípidos en la capa más externa de la micomembrana, en comparación al resto de cultivos de M. brumae y BCG. Estos datos sugieren una clara influencia del medio de cultivo en el perfil de antígenos lipídicos de la pared celular micobacteriana y en la respuesta inmunitaria antitumoral desencadenada. Estos resultados contribuyen a entender cómo las características de las micobacterias son esenciales para crear un microambiente tumoral único que ayuden al sistema inmune a alterar las acciones inmunosupresoras del tumor.
El trabajo se ha llevado a cabo en el Departamento de Genética y de Microbiología en estrecha colaboración de la Fundación Germans Trias i Pujol y el Institut per a la Recerca de la SIDA (IRSI-Caixa), el Instituto de Bioingenieria de Cataluña, la Facultad de Biología de la Universitat de Barcelona, la Unidad de Patología Murina y Comparada de la Facultad de Veterinaria de la UAB, y con la participación de los Servicios de Resonancia Magnética Nuclear y Microscopía de la UAB.
Departamento de Genética y de Microbiología, Facultad de Biociencias, Universitat Autònoma de Barcelona
Referencias
Guallar-Garrido, S., Campo-Pérez, V., Pérez-Trujillo, M., Cabrera, C., Senserrich, J., Sánchez-Chardi, A., Rabanal, R. M., Gómez-Mora, E., Noguera-Ortega, E., Luquin, M., & Julián, E. (2022). Mycobacterial surface characters remodeled by growth conditions drive different tumor-infiltrating cells and systemic IFN-γ/IL-17 release in bladder cancer treatment. Oncoimmunology, 11(1), 2051845. https://doi.org/10.1080/2162402X.2022.2051845
Senserrich, J., Guallar-Garrido, S., Gomez-Mora, E., Urrea, V., Clotet, B., Julián, E., & Cabrera, C. (2022). Remodeling the bladder tumor immune microenvironment by mycobacterial species with changes in their cell envelope composition. Frontiers in immunology, 13, 993401. https://doi.org/10.3389/fimmu.2022.993401


