Descritos defectos genéticos en un enzima asociado a la biosíntesis del coenzima A
En un estudio donde participan investigadores del grupo de Biología Molecular de Levaduras del Instituto de Biotecnologia y Biomedicina (UAB) se ha descrito por primera vez un error congénito ultrarraro en el metabolismo del coenzima A, involucrada en los procesos de obtención de energía en el organismo. Esta investigación crea los cimientos para detectar precozmente el error y poder subsanarlo antes de que cause patología.
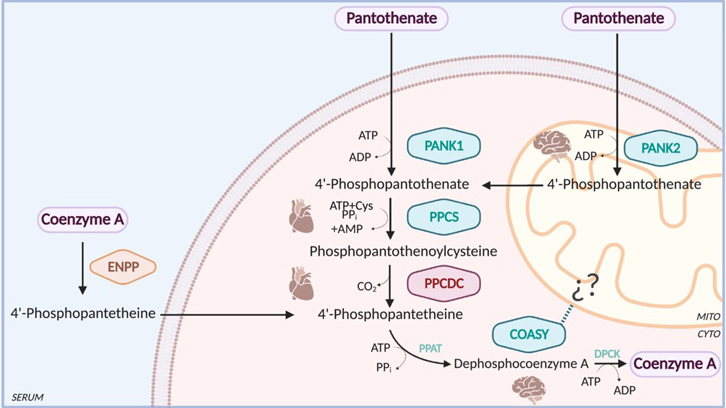
El coenzima A (CoA) es un cofactor esencial involucrado en una gran variedad de procesos metabólicos esenciales para la obtención de energía. Tanto eucariotas como procariotas sintetizan CoA a partir del pantotenato, conocido también como vitamina B5, mediante una vía metabólica casi universal. En humanos, esta vía implica cinco pasos enzimáticos que involucran cuatro enzimas: pantotenato quinasa (PANK), 4’-fosfopantotenoilcisteína sintetasa (PPCS), fosfopantotenoilcisteína descarboxilasa (PPCDC) y CoA sintasa (COASY). Hasta la fecha se conocían defectos genéticos en 3 de los 4 enzimas mencionados, siendo la excepción la PPCDC. En general, estos defectos daban lugar a una patología de carácter severo. La PPCDC codifica una cisteína descarboxilasa que utiliza flavin mononucleótido (FMN) como cofactor y cataliza la descarboxilación de 4’-fosfopantotenoilcisteína a 4’-fosfopanteteína. En los humanos, la forma nativa es un homotrímero de 204 aminoácidos en el que el centro activo se forma en la interfaz de cada dos subunidades.
El primer caso descrito de defectos genéticos asociados a la PPCDC fue publicado recientemente en la revista Journal of Inherited Metabolic Disease a resultas de una colaboración multicéntrica entre diversos laboratorios de Madrid y Valencia que ha contado además con la participación de investigadores de la UAB. Se trata de un caso detectado en dos hermanas, que presentaron severos problemas cardiacos y fallecieron a muy corta edad, que se pudo asociar a variantes bialélicas (p.Thr53Pro y p.Ala95Val) de la PPCDC. Estas variantes afectan a residuos altamente conservados a través de diferentes especies; p.Thr53Pro está involucrado en la unión del mononucleótido de flavina, y p.Ala95Val es probablemente una mutación desestabilizadora. Como resultado, los fibroblastos derivados de estos pacientes mostraron una ausencia de proteína PPCDC y una reducción de casi el 50% en los niveles de CoA. Ademáslas células presentaban claros problemas de carencia energética acompañados de defectos en la respiración mitocondrial.
Estos resultados fueron respaldados por los experimentos realizados empleando un modelo de levaduras deficitario en PPCDC y, por lo tanto, en la biosíntesis de CoA, puesto a punto por el grupo de Biología Molecular de Levaduras del Instituto de Biotecnologia y Biomedicina (UAB) y dirigido por el Dr. Joaquín Ariño. Se trata, por consiguiente, de un trabajo que describe por vez primera un nuevo y ultrarraro error congénito del metabolismo, de graves consecuencias, causado por variantes patogénicas de la PPCDC. De esta manera, se sientan las bases para una posible detección precoz que permitiría una terapia de suplementación que soslayara la deficiencia en PPCDC.
Este trabajo pone también de manifiesto la importancia de los estudios colaborativos multidisciplinarios en la elucidación de las bases genéticas de las enfermedades ultrarraras y enfatiza la importancia del desarrollo de modelos de investigación en eucariotas unicelulares, como las levaduras, cuya aplicación resulta clave en la investigación de sistemas más complejos.
Departament de Bioquímica i Biologia Molecular, Universitat Autònoma de Barcelona.
Institut de Biotecnologia i Biomedicina (IBB-UAB), Universitat Autònoma de Barcelona.
Referencias
Bravo-Alonso I, Morin M, Arribas-Carreira L, Álvarez M, Pedrón-Giner C, Soletto L, Santolaria C, Ramón-Maiques S, Ugarte M, Rodríguez-Pombo P, Ariño J, Moreno-Pelayo MÁ, Pérez B. Pathogenic variants of the coenzyme A biosynthesis-associated enzyme phosphopantothenoylcysteine decarboxylase cause autosomal-recessive dilated cardiomyopathy. J Inherit Metab Dis. 2022 Dec 23. doi: 10.1002/jimd.12584. Epub ahead of print. PMID: 36564894.


