Las células tumorales favorecen su propio crecimiento
Un equipo de investigadores de la Universitat Autònoma ha descubierto un proceso mediante el cual las células cancerígenas favorecen su crecimiento según la composición del medio que las rodea. La elevada presencia de ciertas glucoproteínas, como el versicano, en la matriz extracelular, favorece estos procesos de expansión cancerígena. Los investigadores han encontrado que la propia célula tumoral incrementa la producción de esta glucoproteína. Gracias a la clonación y secuenciación de la región del DNA que regula la producción de versicano, han podido identificar los responsables de su transcripción. La importancia de este descubrimiento reside en el control que se puede lograr de los procesos de regulación genética, lo que puede permitir un avance importante en la lucha contra el cáncer.
El crecimiento de un tumor está gobernado no sólo por el potencial de las células tumorales sino también por la matriz extracelular que las rodea. La propia célula tumoral modifica la composición de esta matriz para hacerla más favorable a la expansión del tumor. Uno de los componentes de la matriz extracelular que se incrementa notablemente es un proteoglicano llamado VERSICANO. Los proteoglicanos son un tipo especial de glucoproteínas que se caracterizan por tener una parte glucídica importante. En este trabajo hemos descrito cuáles son las vías de regulación que controlan la expresión del versicano en líneas celulares de melanoma humano.
La estrategia que hemos seguido ha sido clonar y secuenciar el promotor del versicano humano, es decir, la región del gen que está próxima a la parte que contiene la secuencia del promotor y consultando las bases de datos adecuadas, hemos identificado las posibles secuencias reguladoras y los factores de transcripción, es decir, las proteínas reguladoras que se unen.
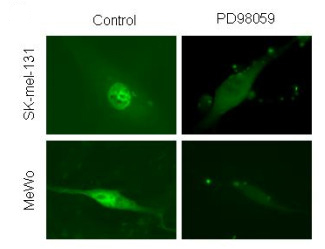
Uno de los factores de transcripción que tiene un papel más protagonista en la regulación de la expresión del versicano es el llamado AP-1. Este factor de transcripción AP-1 se activa en respuesta a determinados factores de crecimiento y oncogenes. Uno de los oncogenes con capacidad de activar a AP-1 es el oncogen B-Raf, que se encuentra muy frecuentemente mutado y, en consecuencia, activado en el caso del melanoma. La activación de B-Raf lleva como consecuencia la activación de la cascada de señalización de las proteínas quinasas de la familia ERK, una de las vías esenciales que controlan la proliferación celular.
El otro factor de transcripción que contribuye de manera importante a la regulación de la expresión del versicano es el llamado TCF-4. Este factor es un componente de la vía de señalización de la beta-catenina, que está también frecuentemente activada en muchos tipos de tumores. Así, en los casos en que AP-1 y TCF-4 están activados como consecuencia de mutaciones en oncogenes o por otras causas, la producción de versicano será alta y favorecerá la expansión del tumor.
Para llegar a estas conclusiones, hemos usado toda una serie de técnicas moleculares diferentes: clonaje y secuenciación, preparación de constructos que contiene regiones específicas del promotor, mutagénesis dirigida, transfección de las células de melanoma con estos constructos y visualización de la actividad del promotor, técnicas de retraso en gel, western blot, inmunocitoquímica. La utilización del método científico, es decir, trabajar a partir de una hipótesis y con la combinación adecuada de técnicas para comprobarla, permite llegar a encontrar respuestas a preguntas complejas que nos den luz sobre las alteraciones que sufre una célula cuando se transforma en cancerosa.
Referencias
"Structure and regulation of the versican promoter: the versican promoter is regulated by AP-1 and TCF transcription factors in invasive human melanoma cells". Clelia Domenzain-Reyna, Daniel Hernández, Laia Miquel-Serra, María José Docampo, Celia Badenas, Angels Fabra, Anna BassolsJournal of Biological Chemistry, 284(18):12306-17, 2009.


