Barrejant cations de cobalt amb cadenes de glicina dins d'un ordinador
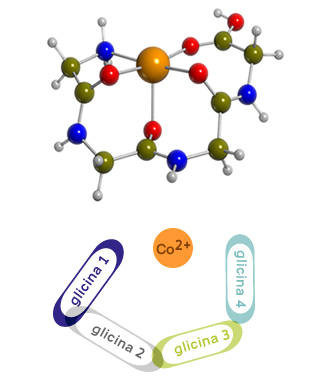
Un grup de recerca, format per químics de la UAB, ha simulat per ordinador les estructures tridimensionals més estables de certes biomolècules de cobalt. Aquestes consisteixen en pèptids coordinats a l'àtom metàl·lic però, per tal d'afavorir els càlculs computacionals, han simplificat el sistema considerant els aminoàcids més senzills com la glicina. Els resultats apunten a un increment en el nombre de coordinació del metall en augmentar la llargària de la cadena, pel cas del Co2+, mentre que pel catió Co+ l'estructura més afavorida és tricoordinada.
Molts processos biològicament importants requereixen la participació d’un catió metàl·lic i impliquen la interacció d’aquest amb les biomolècules que es troben als éssers vius. En molts casos intervenen les proteïnes, cadenes formades per unitats (aminoàcids) que es van enllaçant entre elles, com les baules d’una cadena. El tipus d’aminoàcids i la manera en la que s’uneixen determinen la forma i la funció de la proteïna. Cal dir que els aminoàcids s’enllacen a través dels mateixos àtoms, formant un tipus d’unió anomenada enllaç peptídic. A més, contenen àtoms (normalment nitrogen (N), oxigen (O) o sofre (S)) que poden actuar com a punt d’ancoratge (d’interacció) dels cations metàl·lics. La preferència dels cations metàl·lics per uns o altres àtoms del pèptid dependrà de llur naturalesa química (no és el mateix un catió de Fe3+ que un de Zn2+), així com el nombre d’àtoms que envolten el catió.
Així, quant més gran és el pèptid (la cadena d’aminoàcids), més punts d’interacció presenta; per tant, més possibilitats diferents d’interacció del catió (més possibilitats d’estructures diferents). D’aquestes, sol haver-ne una, o unes poques, que són les més favorables, les més estables. Poder conèixer-les i estudiar el tipus d’interacció que s’hi estableix entre el catió i el pèptid pot ser de gran ajuda per entendre millor la importància biològica dels cations metàl·lics. Tot i això, la grandària d’una proteïna fa inviable aquest estudi mitjançant tècniques computacionals, per la qual cosa, un primer pas seria l’estudi de la interacció d’un catió metàl·lic amb pèptids petits constituïts per diferents aminoàcids o únicament per glicina, ja que és l’aminoàcid més petit. Aquests tipus de treballs han experimentat un creixement en les darreres dues dècades gràcies, no sols als avenços de la informàtica (tècniques computacionals), sinó també als avenços en l’espectrometria de masses.
En aquest article hem estudiat la interacció dels cations metàl·lics de Cobalt Co+ i Co2+ amb tres pèptids petits de glicina, els quals contenen des de 2 fins a 4 unitats d’aquest aminoàcid. El motiu de l’elecció d’aquests cations és doble. Des del punt de vista químic i computacional, perquè poden presentar diferents estats electrònics; és a dir, diverses maneres de distribuir els electrons en els orbitals. Suposem que tenim 5 habitatges, que poden trobar-se buits o habitats per un o per 2 inquilins. Cada habitatge representaria un orbital i cada inquilí, un electró. El Co+ té 8 electrons per distribuir, 8 inquilins, que es podrien distribuir de les següents maneres: a) 3 habitatges amb 2 inquilins i dos pisos amb sols una persona en cadascun o, b) 4 habitatges plens i 1 de completament de buit. Les dues situacions (triplet i singlet, respectivament) correspondrien a dos estats electrònics diferents a nivell químic. Habitualment un estat és més estable que l’altre. En el cas del Co2+, hi hauria 7 electrons per distribuir. A més, aquests dos cations presenten una importància biològica: el Co2+ es troba a les cobalamines, com la vitamina B12, mentre que el Co+ participa en alguns dels processos de les cobalamines. Tot i que, en determinades concentracions, també poden resultar tòxics.
L’objectiu d’estudiar la interacció de cadenes de glicina amb cations de Cobalt és la de determinar com són les estructures més estables, els punts d’interacció, així com l’energia d’interacció entre el catió i el pèptid, tot això mitjançant eines computacionals (emprant mètodes del funcional de la densitat). Per a les tres cadenes escollides s’ha trobat que, per al Co+, l’estat electrònic més estable és sempre el triplet i les estructures més afavorides de tipus tricoordinat: el catió interacciona amb 3 àtoms de la cadena, normalment oxígens. Per al Co2+ però, el nombre d’àtoms que interaccionen amb el catió augmenta a l’augmentar la llargada de la cadena. Per a ambdós cations, l’allargament de la cadena de glicines repercuteix en un increment de l’energia d’interacció (cal més energia per trencar els seus enllaços). Així doncs, la química computacional permet l’obtenció d’informació valuosa sobre l’estructura de molècules i complexos.
Referències
"Coordination of (Glycyl)(n)glycine (n=1-3) to Co+ and Co2+". Constantino, Erika; Rimola, Albert; Sodupe, Mariona; Rodríguez-Santiago, Luis. JOURNAL OF PHYSICAL CHEMISTRY A, 113 (31): 8883-8892 AUG 6 2009.


